Дихлорацетат (ДХА) и рак: обзор клинического применения
Дихлорацетат (ДХА) и рак: обзор клинического применения
Лаборатория доклинических и трансляционных исследований, IRCCS-CROB, Реферальный онкологический центр Базиликаты, Рионеро-ин-Вультуре (Pz), 85028, Италия
2 Кафедра клинической и экспериментальной медицины, Университет Фоджи, Фоджа 71121, Италия
Корреспонденцию следует направлять Тициане Татарани; tiziana.tataranni@crob.it
Приглашенный редактор: Канхайя Сингх
Авторские права © 2019 Тициана Татаранни и Клаудия Пикколи. Это статья открытого доступа, распространяемая по лицензии Creative Commons Attribution, которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии надлежащего цитирования оригинальной работы.
Получено: 24 июля 2019 г.
Изменено: 12 сентября 2019 г.
Принято: 11 октября 2019 г.
Опубликовано онлайн: 14 ноября 2019 г.
Обширный объем литературы описывает противораковые свойства дихлорацетата (DCA), но его эффективное клиническое применение в терапии рака по-прежнему ограничивается клиническими испытаниями. Возникновение побочных эффектов, таких как нейротоксичность, а также подозрение на канцерогенность DCA по-прежнему ограничивают клиническое применение DCA. Однако в последние годы число отчетов, поддерживающих использование DCA против рака, возросло также из-за большого интереса к нацеливанию на метаболизм опухолевых клеток. Анализ механизма действия DCA помог понять основы его селективной эффективности против раковых клеток. Успешное совместное введение DCA с традиционной химиотерапией, радиотерапией, другими препаратами или природными соединениями было протестировано на нескольких моделях рака. Новые системы доставки лекарств и многофункциональные соединения, содержащие DCA и другие препараты, по-видимому, улучшают биодоступность и кажутся более эффективными благодаря синергетическому действию нескольких агентов. Распространение отчетов, поддерживающих эффективность DCA в терапии рака, побудило провести дополнительные исследования, которые позволили найти другие потенциальные молекулярные мишени DCA. Интересно, что DCA может существенно влиять на фракцию стволовых клеток рака и способствовать искоренению рака. В совокупности эти результаты дают весомое обоснование для новых клинических трансляционных исследований DCA в терапии рака.
ВВЕДЕНИЕ
Рак является одной из основных причин смерти во всем мире. Несмотря на значительный прогресс в диагностических и терапевтических подходах, его искоренение по-прежнему представляет собой проблему. Слишком много факторов ответственны за неудачу терапии или рецидив, поэтому существует острая необходимость в поиске новых подходов к его лечению. Помимо типичных известных свойств, характерных для злокачественных клеток, включая аномальную пролиферацию, дерегуляцию апоптоза и клеточного цикла [1, 2] , раковые клетки также демонстрируют особую метаболическую машину, которая предлагает еще один многообещающий подход к терапии рака [3–5] . Наша группа уже предположила важность метаболической характеристики раковых клеток для прогнозирования эффективности метаболического лечения [6] . Лекарства, способные влиять на метаболизм рака, уже рассматриваются, показывая обнадеживающие результаты с точки зрения эффективности и переносимости [7] . В последнее десятилетие малая молекула DCA, уже используемая для лечения острого и хронического лактоацидоза, врожденных ошибок митохондриального метаболизма и диабета [8] , в основном предназначалась в качестве противоракового препарата. DCA представляет собой водорастворимую молекулу кислоты массой 150 Да, аналог уксусной кислоты, в которой два из трех атомов водорода метильной группы заменены атомами хлора (рисунок 1(a)) [9] . Введение DCA в дозах от 50 до 200 мг/кг/умер связано с уменьшением объема опухолевой массы, скорости пролиферации и распространения метастазов в нескольких доклинических моделях [10] . Наша группа уже наблюдала обратную корреляцию между способностью DCA убивать раковые клетки и их митохондриальной дыхательной способностью в карциномах ротовых клеток [11] . Более того, недавно мы описали способность DCA влиять на митохондриальную функцию и замедлять прогрессирование рака в модели рака поджелудочной железы [12] . На сегодняшний день доступны последовательные данные клинических испытаний и отчеты о случаях, описывающие введение DCA у онкологических больных [13–16] , но, несмотря на растущий объем литературы, подтверждающей эффективность DCA против рака, он пока не используется в клинической практике. Целью этого обзора является обобщение последних отчетов, предполагающих использование DCA в терапии рака в сочетании с химиотерапевтическими агентами, радиотерапией и другими химическими или природными соединениями, демонстрирующими противораковые свойства. Кроме того, мы описали данные о новых целевых фармакологических формулах DCA, способных избегать побочных эффектов и улучшать биодоступность и эффективность препарата, что еще больше поощряет его возможное клиническое применение. Наконец, мы рассмотрели последние результаты, предполагающие другие потенциальные механизмы действия DCA, включая новые данные о его способности влиять на фракцию стволовых клеток рака.
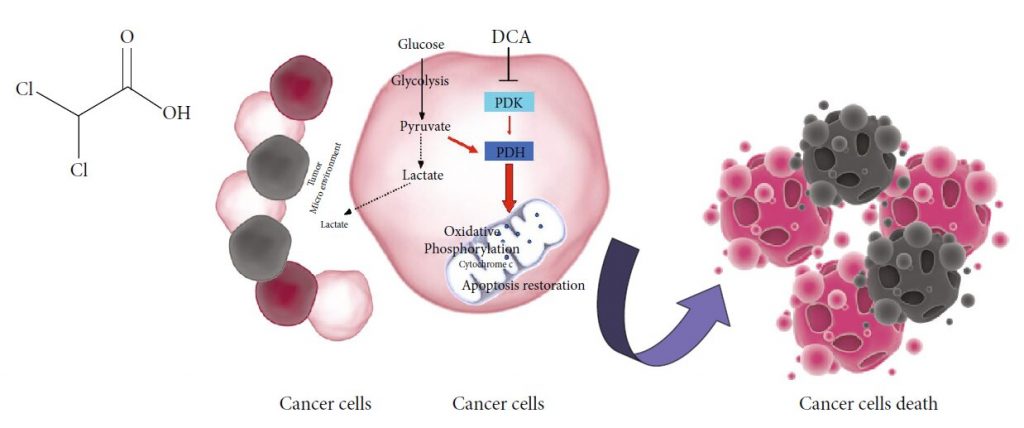 Рисунок 1: (a) Химическая структура DCA. (b) Механизм действия DCA: PDK: пируватдегидрогеназная киназа; PDH: пируватдегидрогеназа. Черные пунктирные линии — биохимические процессы, ингибируемые DCA; Красные стрелки — метаболические пути, активируемые DCA.
Рисунок 1: (a) Химическая структура DCA. (b) Механизм действия DCA: PDK: пируватдегидрогеназная киназа; PDH: пируватдегидрогеназа. Черные пунктирные линии — биохимические процессы, ингибируемые DCA; Красные стрелки — метаболические пути, активируемые DCA.
DCA и рак: механизм действия
Потенциальная эффективность DCA в терапии рака обусловлена метаболическими свойствами раковых клеток, которые обычно характеризуются повышенной гликолитической активностью и сниженным митохондриальным окислением независимо от доступности кислорода, хорошо известный эффект Варбурга [17] . Чрезмерный гликолиз и возникающее в результате перепроизводство лактата вызывают состояние метаболического ацидоза в микроокружении опухоли [ 18] . Лактат, образующийся в результате гликолиза, поглощается окружающими клетками для поддержки роста опухоли и ингибирует механизмы апоптотической гибели клеток [19, 20] . Несколько ферментов, участвующих в гликолизе, регулируют апоптоз, и их сверхэкспрессия в раковых клетках способствует подавлению апоптоза [21] . В этой ситуации соли DCA избирательно воздействуют на раковые клетки, переключая их метаболизм с гликолиза на окислительное фосфорилирование путем ингибирования киназы пируватдегидрогеназы (PDK), ингибитора пируватдегидрогеназы (PDH) [10] . Активация PDH способствует митохондриальному окислению пирувата и нарушает метаболическое преимущество раковых клеток. Мутации митохондриальной ДНК, часто возникающие при опухолеобразовании и приводящие к дисфункции дыхательной цепи [22, 23] , делают злокачественные клетки неспособными поддерживать клеточную потребность в энергии. Кроме того, снижая выработку лактата, DCA противодействует ацидозному состоянию микроокружения опухоли, способствуя ингибированию роста опухоли и ее распространению [24] . Доставка пирувата в митохондрии вызывает ремоделирование органелл, что приводит к увеличению оттока цитохрома c и других факторов, индуцирующих апоптоз, и повышению уровня ROS с последующим снижением жизнеспособности раковых клеток [9] (рисунок 1(b)).
Побочные эффекты и ограничения при использовании DCA
Клиническое применение DCA доступно как в пероральных, так и в парентеральных формулах, а дозы варьируются от 10 до 50 мг/кг/смерть [25] . Никакие доказательства тяжелой гематологической, печеночной, почечной или сердечной токсичности не подтверждают безопасность DCA [26] . Распространенные желудочно-кишечные побочные эффекты часто возникают у определенного процента пациентов, получавших лечение DCA [15] . Наиболее известным ограничением для введения DCA, наблюдавшимся как в доклинических, так и в клинических исследованиях, является периферическая невропатия [27] . Избирательность повреждения нервной системы, вызванного DCA, может быть связана с отсутствием хорошо оснащенного аппарата, способного справиться с более устойчивым окислительным фосфорилированием в клетках, продуцирующих АТФ в основном посредством гликолиза [28] . Возникающая в результате перегрузка митохондрий ставит под угрозу эффективность антиоксидантных систем, неспособных противостоять чрезмерному количеству ROS. В этой ситуации современное введение антиоксидантов должно представлять собой дополнительную стратегию для минимизации невропатии, вызванной DCA [27] . Экспрессия и активность глутатионтрансферазы zeta1 (GSTZ1), первого фермента, ответственного за клиренс DCA, могут влиять на сущность повреждения. Несинонимичные функциональные однонуклеотидные полиморфизмы (SNP) в гене человека GSTZ1 приводят к появлению различных гаплотипов, которые отвечают за различную кинетику и динамику DCA. Была продемонстрирована четкая связь между гаплотипом GSTZ1 и клиренсом DCA. На этой основе персонализированная дозировка DCA, основанная не только на массе тела, может минимизировать или предотвратить побочные эффекты у пациентов, хронически принимающих этот препарат [29] . Возникновение нейропатии связано с хроническим пероральным приемом DCA и является обратимым эффектом, ограниченным временем лечения [30] . Внутривенный путь снижает, OH Cl Cl O (a) Раковые клетки Раковые клетки Смерть раковых клеток Лактат Опухоль Микросреда Лактат Пируват Гликолиз PDK DCA PDH Окислительное фосфорилирование Апоптоз восстановление Цитохром c Глюкоза (b) Рисунок 1: (a) Химическая структура DCA. (b) Механизм действия DCA: PDK: пируватдегидрогеназная киназа; PDH: пируватдегидрогеназа. Черные пунктирные линии, биохимические процессы, ингибируемые DCA; Красные стрелки, метаболические пути, активируемые DCA. 2 Окислительная медицина и клеточная продолжительность жизни, следовательно, потенциал нейротоксичности и позволяют достижению более высоких концентраций препарата обойти пищеварительную систему [13] .
Поскольку DCA входит в число побочных продуктов дезинфекции воды, обнаруженных в низких концентрациях в питьевой воде, его потенциальная канцерогенность находится на стадии оценки. Исследования, проведенные на мышах, связывают воздействие DCA в раннем возрасте с увеличением частоты возникновения гепатоцеллюлярных опухолей [31]. Вполне возможно, что постоянные изменения в метаболизме клеток, вызванные DCA, могут вызывать эпигенетические эффекты. Длительная индукция PDH и других окислительных путей, связанных с метаболизмом глюкозы, может способствовать увеличению активных форм кислорода и митохондриального стресса [27] . Однако в клинических исследованиях не сообщается о каких-либо доказательствах канцерогенного эффекта при введении DCA в терапии рака.
Синергетический эффект DCA и химиотерапевтических агентов
Комбинирование различных препаратов является общепринятой стратегией для получения синергического полезного эффекта в терапии рака, снижения дозировки препаратов, минимизации рисков токсичности и преодоления лекарственной устойчивости. Совместное введение DCA и традиционных химиотерапевтических агентов было предназначено и протестировано на нескольких моделях рака (таблица 1). Лечение DCA, по-видимому, повышает эффективность химиотерапии, вызывая биохимические и метаболические изменения, что приводит к значительным изменениям энергетического баланса раковых клеток. Исследование, проведенное при немелкоклеточном раке легких (НМРЛ), показало как in vitro, так и in vivo, что совместное введение DCA с паклитакселом повышает эффективность гибели клеток за счет ингибирования аутофагии [32] . Эффективная комбинация DCA и доксорубицина (DOX) была протестирована на клетках HepG2, продемонстрировав способность DCA нарушать клеточную антиоксидантную защиту, тем самым способствуя окислительному повреждению, в свою очередь, вызванному лечением DOX [33] . Существует сильная связь между сверхэкспрессией PDK и химиорезистентностью; таким образом, можно предположить, что ингибирование PDK может помочь повторно сенсибилизировать раковые клетки к препаратам. Сверхэкспрессия изоформы PDK2 была связана с резистентностью к паклитакселу при НМРЛ. Интересно, что комбинация DCA с паклитакселом была более эффективна в уничтожении резистентных клеток, чем лечение паклитакселом или DCA по отдельности [34] . Подобно НМРЛ, интересное исследование in vivo, проведенное при распространенном раке мочевого пузыря, показало повышенную экспрессию изоформы PDK4 при высокой степени злокачественности по сравнению с раком низкой степени злокачественности, а совместное лечение DCA и цисплатином значительно уменьшило объемы опухоли по сравнению с DCA или цисплатином по отдельности [35]. Недавнее исследование подтвердило способность DCA устранять химиорезистентность, связанную с PDK4, также при гепатоцеллюлярной карциноме человека (ГЦК) [36] .
| Опухолевая сущность | Модельная система | Препарат химиотерапии, вводимый совместно с DCA | Механизм действия | Исход | Ссылки |
| Рак легких | Линии клеток A549-H1975/модель ксенотрансплантата | Паклитаксел | Торможение аутофагии | Эффективная сенсибилизация к химиотерапии рака | [32] |
| Гепатокарцинома | Линия клеток HepG2 | Доксорубицин | Нарушение антиоксидантной защиты | Увеличение повреждения клеток из-за индукции окислительного стресса | [33] |
| Рак легких | Линия клеток A549 | Паклитаксел | Повышенная химиочувствительность за счет ингибирования PDK2 | Преодоление резистентности к паклитакселу | [34] |
| Рак мочевого пузыря | Клеточные линии HTB-9, HT-1376, HTB-5, HTB-4/модель ксенотрансплантата | Цисплатин | Повышенная химиочувствительность за счет ингибирования PDK4 | Увеличение гибели раковых клеток и потенциальные терапевтические преимущества | [35] |
| Гепатокарцинома | Сферические культуры из клеточных линий HepaRG и BC2 | Цисплатин, сорафениб | Повышенная химиочувствительность за счет ингибирования PDK4 | Улучшение терапевтического эффекта химиотерапии за счет восстановления активности митохондрий | [36] |
Таблица 1: Список отчетов, предполагающих положительный эффект совместного применения DCA и химиотерапии при нескольких типах рака.
Синергетический эффект DCA и других потенциальных противораковых препаратов
Последовательный объем литературы предполагает положительные эффекты совместного введения DCA с соединениями, которые в настоящее время используются для лечения других заболеваний, но демонстрируют противораковые свойства в нескольких моделях рака (таблица 2). Современное введение DCA и антибиотика салиномицина, недавно заново открытого за его цитотоксические свойства как потенциального противоракового препарата, было протестировано на линиях клеток колоректального рака. Их лечение, по-видимому, оказывает синергический цитотоксический эффект, ингибируя экспрессию белков, связанных с множественной лекарственной устойчивостью [37] . Раковые клетки, лишенные метаболических ферментов, участвующих в метаболизме аргинина, могут привести к чувствительности к лечению аргиназой. Интересно, что совместное введение рекомбинантной аргиназы и DCA оказывает антипролиферативный эффект при тройном негативном раке молочной железы из-за активации p53 и индукции остановки клеточного цикла [38] . Ингибиторы COX2, в основном используемые в качестве противовоспалительных препаратов, недавно были предложены в качестве противоопухолевых препаратов из-за их антипролиферативной активности. Интригующее исследование, проведенное на клетках рака шейки матки, показало неспособность DCA убивать клетки рака шейки матки, сверхэкспрессирующие COX2, и продемонстрировало, что ингибирование COX2 целекоксибом делает клетки рака шейки матки более чувствительными к DCA как в экспериментах in vitro, так и in vivo [39] . Поскольку DCA способствует окислительному фосфорилированию за счет снижения гликолитической активности, сочетание DCA с другими препаратами, усиливающими состояние зависимости от глюкозы, может быть многообещающей стратегией. Такой подход был опробован при раке головы и шеи, при котором введение пропранолола, неселективного бета-блокатора, способного влиять на митохондриальный метаболизм опухолевых клеток, вызывало гликолитическую зависимость и энергетический стресс, делая клетки более уязвимыми для лечения DCA [40] . Аналогичные результаты были получены в клетках меланомы, в которых введение ингибиторов рецептора ретиноевой кислоты β (RARβ) вызывало сенсибилизацию к DCA [41] . Положительный эффект совместного введения DCA с метформином, гипогликемическим препаратом, широко используемым для лечения диабета, был продемонстрирован в доклинической модели глиомы [42] , а также в низкометастатическом варианте карциномы легких Льюис (LLC) [43] . Цзян и его коллеги исследовали эффекты фенформина, аналога метформина, и DCA в глиобластоме, продемонстрировав, что одновременное ингибирование комплекса I и PDK фенформином и DCA, соответственно, снижало самообновление и жизнеспособность стволовых клеток глиомы (GSC), что предполагает их возможное использование для воздействия на фракцию стволовых клеток рака [44] .
| Лекарство | Основная функция | Опухолевая сущность | Модельная система | Исход | Ссылки |
| Салиномицин | Антибиотик | Колоректальный рак | Линии клеток DLD-1 и HCT116 | Ингибирование белков, связанных с множественной лекарственной устойчивостью | [37] |
| Аргиназа | Метаболизм аргинина | Рак молочной железы | Модель MDA-MB231 и MCF-7/ксенотрансплантат | Антипролиферативный эффект за счет активации p53 и остановки клеточного цикла | [38] |
| ингибиторы ЦОГ2 | Воспаление | Рак шейки матки | Линии клеток HeLa и SiHa/модель ксенотрансплантата | Подавление роста раковых клеток | [39] |
| Пропранолол | Бета-блокатор | Рак головы и шеи | Клеточные линии mEERL и MLM3/C57Bl/6 м | Повышение глюкозозависимости и усиление эффекта химиолучевой терапии | [40] |
| Ингибиторы RARβ | Метаболизм витамина А | Меланома | Клеточные линии ED-007, ED-027, ED-117 и ED196 | Развитие зависимости от глюкозы и сенсибилизация к DCA | [41] |
| Метформин | Диабет | Глиома, карцинома легких Льюиса | Модель ксенотрансплантата; клетки LLC/R9 | Продление жизни мышей с глиомой; сильная зависимость от глюкозы в микроокружении опухоли | [42, 43] |
| Фенформин | Диабет | Глиобластома | Модель стволовых клеток глиомы/ксенотрансплантата | Торможение самообновления раковых стволовых клеток | [44] |
Таблица 2: Список препаратов, основная функция которых была протестирована в сочетании с DCA на нескольких моделях рака.
Совместное использование DCA и натуральных соединений
Клиническое применение природных соединений представляет собой многообещающий новый подход к лечению ряда заболеваний [45] . Все больше литературы подтверждает обнаружение среди природных соединений биологически активных веществ, выделенных растениями, грибами, бактериями или морскими организмами, которые оказывают благотворное воздействие на здоровье человека [46–48] . Предположение о природных соединениях или их производных, по-видимому, представляет собой обнадеживающий подход к предотвращению возникновения или рецидива рака, и это обычно называется химиопрофилактикой [49] . Более того, природные вещества оказывают благотворное воздействие при терапии рака при совместном введении с другими препаратами, демонстрируя их способность преодолевать лекарственную устойчивость, увеличивать противораковый потенциал и снижать дозы лекарств и токсичность [50, 51] . Интересно, что недавно было предложено совместное введение DCA и природных соединений. В исследовании изучалось комбинированное действие DCA с куркумином, смешанным с эфирным маслом, соединением с полезными свойствами как для профилактики, так и для лечения рака [52] , демонстрирующим противораковый потенциал против HCC [53] . В частности, сочетание обоих соединений синергически снижало выживаемость клеток, способствуя апоптозу клеток и вызывая внутриклеточную генерацию ROS. Бетулин, природное соединение, выделенное из бересты, уже известно своим антипролиферативным и цитотоксическим действием против нескольких линий раковых клеток [54–56] . Исследование противоопухолевой активности производных бетулина in vitro при НМРЛ подтвердило его способность ингибировать in vivo и in vitro рост клеток рака легких, блокируя фазу G2/M клеточного цикла и вызывая активацию каспазы и фрагментацию ДНК. Интересно, что производное бетулина Bi-L-RhamBet было способно нарушать митохондриальную электрон-транспортную цепь (ETC), вызывая выработку ROS. Учитывая свойство DCA увеличивать общее окисление глюкозы в митохондриях через цикл Кребса и ETC, авторы объединили Bi-L-RhamBet с DCA, продемонстрировав его значительную потенцированную цитотоксичность [57] .
DCA и радиосенсибилизация
Радиотерапия представляет собой еще одну стратегию лечения рака и обеспечивает локальный подход путем введения высокоэнергетических лучей [58] . Основным эффектом облучения является индукция ROS с последующим повреждением ДНК, хромосомной нестабильностью и гибелью клеток путем апоптоза [59] . Однако некоторые опухоли демонстрируют или развивают радиорезистентность, которая является причиной неудачи радиотерапии и высокого риска рецидива опухоли или метастазирования [60] . Несколько факторов могут быть ответственны за радиорезистентность [61] . Среди них гипоксия, распространенное состояние микросреды опухоли, характеризующееся низким уровнем кислорода и сниженной генерацией видов ROS, может блокировать эффективность ионизирующего излучения [62] . Поэтому увеличение оксигенации опухоли таким образом, чтобы способствовать значительному количеству ROS [63] или напрямую индуцировать выработку ROS, может представлять собой стратегию повышения радиосенсибилизации [64 , 65] . В этой ситуации введение DCA, которое, как известно, индуцирует выработку ROS [11, 66] , может представлять собой стратегию преодоления радиорезистентности опухоли. Более того, известно, что метаболические изменения, характерные для развития рака, влияют на радиочувствительность [67, 68] . Следовательно, нацеливание на промежуточные продукты метаболизма рака может представлять собой стратегию улучшения селективного ответа рака на облучение [69] . Эффективность DCA для повышения радиочувствительности уже была продемонстрирована как на клетках глиобластомы [70] , так и на плоскоклеточной карциноме пищевода [71] . Совсем недавно было продемонстрировано, что DCA повышает радиочувствительность в клеточной модели медуллобластомы, смертельной опухоли мозга у детей, вызывая изменения метаболизма ROS и функции митохондрий и подавляя способность к восстановлению ДНК [72] . Поскольку роль иммунотерапии в восстановлении иммунной защиты против прогрессирования опухоли и метастазирования привлекает большое внимание в последние годы [73] , Гупта и Двараканат представили современное состояние возможных эффектов гликолитических ингибиторов, включая DCA, на радиосенсибилизацию опухоли, сосредоточив свое внимание на взаимодействии между метаболическими модификаторами и иммунной модуляцией в процессах радиосенсибилизации [74] . Интересно, что они сообщили о способности DCA способствовать иммунной стимуляции посредством ингибирования накопления лактата, что еще больше поддерживает его использование в качестве адъюванта радиотерапии.
DCA и новые лекарственные формы
Растет интерес к разработке новых лекарственных форм для улучшения доставки лекарств, повышения эффективности и снижения доз и, следовательно, нежелательных эффектов. В этой ситуации системы доставки лекарств (СДЛ) представляют собой новый рубеж в современной медицине [75] . СДЛ предлагают возможность создания гибрида металлоорганических каркасов (МОФ), сочетающего биосовместимость органической системы с высокими нагрузками неорганической фракции [76] . Несколько линий доказательств предполагают эффективную функционализацию наночастиц с помощью ДКА. Лазаро и коллеги [77] исследовали различные протоколы для функционализации ДКА наночастиц терефталата циркония (Zr) (UiO-66). Они продемонстрировали цитотоксичность и селективность тех же СДЛ против различных линий раковых клеток. Более того, они исключили возможную реакцию иммунной системы на ДКА-МОФ in vitro. Та же группа позже показала возможность загрузки Zr MOF вторым противораковым препаратом, таким как 5-фторурацил (5-FU), чтобы воспроизвести синергический эффект двух препаратов [78] . MOF на основе циркония, загруженный DCA, также был предназначен в качестве привлекательной альтернативы UiO-66, показывая селективную цитотоксичность in vitro по отношению к нескольким линиям раковых клеток и хорошую переносимость иммунной системой нескольких видов [79] . Недавно Štarha et al. [80] впервые синтезировали и охарактеризовали полусэндвич-комплексы, содержащие рутений или осмий и DCA (рисунок 2(a)). Оба комплекса Ru-dca и Os-DCA были проверены на линиях клеток карциномы яичников, продемонстрировав большую цитотоксичность, чем цисплатин в отдельности. Оба комплекса были способны индуцировать высвобождение цитохрома c (Cytc) из митохондрий, косвенный показатель активации апоптосомы, и, по-видимому, были менее токсичными по отношению к здоровым первичным гепатоцитам человека, что указывает на селективность в отношении рака по сравнению с нераковыми клетками. Многообещающие результаты были также получены в клетках рака молочной железы с тройным негативом [81] . Конъюгат рения (I)-DCA продемонстрировал эффективное проникновение в раковые клетки и селективное накопление в митохондриях, вызывая митохондриальную дисфункцию и метаболические нарушения [82] . В последние годы было разработано несколько многоактивных препаратов для современного нацеливания на различные внутриклеточные пути с использованием одной формулы. Безопасная, простая, воспроизводимая наноформула комплекса доксорубицинDCA (рисунок 2(b)) была успешно испытана на модели меланомы у мышей, показав увеличение способности к загрузке препарата, снижение побочных эффектов и усиление терапевтического эффекта [83] . Были синтезированы противоопухолевые пролекарства Pt (IV) двойного действия китеплатина с аксиальными лигандами DCA (рисунок 2(c)), охарактеризованы и протестированы на различных линиях опухолевых клеток и in vivo [84]. Для преодоления резистентности рака были предложены тройные производные Pt (IV) цисплатина в качестве новых мощных противораковых агентов, способных конъюгировать действие цисплатина, ингибиторов циклооксигеназы и DCA (рисунок 2(d)) [85] . Новый комплекс, содержащий DCA, платину и биотин (DPB), был успешно испытан, демонстрируя многогранные противоопухолевые свойства (рисунок 2(e)). Авторы продемонстрировали способность такого пролекарства влиять на энергетический метаболизм, способствовать апоптозу и взаимодействовать с ДНК. Высокая селективность биотина в отношении раковых клеток сводит к минимуму пагубное воздействие на нормальные клетки и улучшает лечебный эффект на опухоли [86] . Характеристики и экспериментальные доказательства основных классов соединений обобщены в таблице 3.
| Класс лекарственной формы | Функции | Тесты in vitro | Тесты in vivo | Экспериментальные доказательства | Ссылки |
| Металло-DCA каркасы (без платины) | Ионы металлов, связанные с органическими лигандами в пористые каркасы | MCF-7/MDA-MB-231 (молочная железа) HeLa/LO2 (шейка матки) A2780 (яичник) A549/NCl-H1229 (легкое) | Модели грудных мышей | Биосовместимость, избирательная цитотоксичность, совместимость с иммунной системой, низкая мутагенность. | [77–82 ] |
| Конъюгат доксорубицина-DCA | Комплексы ДХА и химиотерапевтических препаратов | B16F10 (меланома) | Мышиные модели саркомы и меланомы | Безопасность селективной цитотоксичности. Эффективность противоопухолей in vivo. | [83] |
| Платиновые пролекарства с DCA | Платиновое ядро, связанное с DCA и другими препаратами | MCF-7 (молочная железа) LoVo/HCT-15/HCT116 (толстая кишка) A549 (легкие) BxPC3/PSN-1 (поджелудочная железа) A375 (меланома) BCPAP (щитовидная железа) HeLa (шейка матки) HepG2 (гепатокарцинома) | Мышиные модели карциномы легких | Избирательная цитотоксичность, множественное действие. Увеличение клеточного поглощения. | [84–86 ] |
Таблица 3: Свойства основных классов лекарственных форм DCA, протестированные на линиях раковых клеток и моделях in vivo с соответствующими экспериментальными доказательствами.
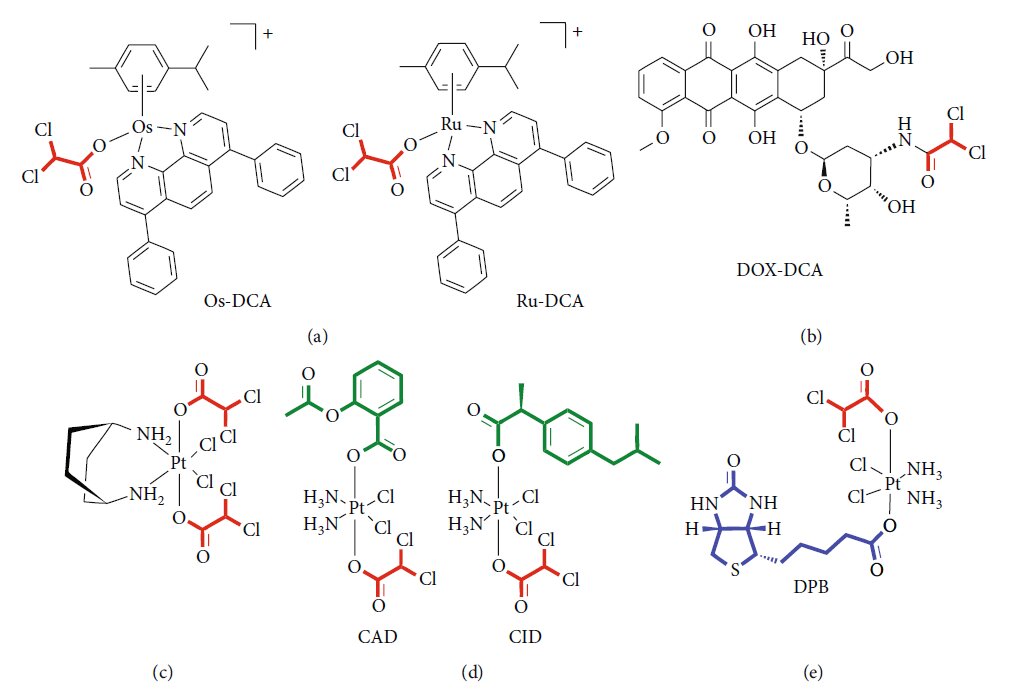 Рисунок 2: Новые лекарственные формы, содержащие DCA. (a) Схематическое изображение комплексов Os-DCA и Ru-DCA [81]. (b) Комплекс доксорубицин (DOX)-DCA [83]. (c) Пролекарства Pt двойного действия китеплатина и DCA [84]. (d) Примеры производных Pt(IV) тройного действия цисплатина, содержащих DCA (красный), производные цисплатина (черный) и ингибиторы COX (зеленый) [85]. (e) Химическая структура DPB, содержащего DCA (красный), биотин (синий) и комплекс платины (Pt) (черный) [86].
Рисунок 2: Новые лекарственные формы, содержащие DCA. (a) Схематическое изображение комплексов Os-DCA и Ru-DCA [81]. (b) Комплекс доксорубицин (DOX)-DCA [83]. (c) Пролекарства Pt двойного действия китеплатина и DCA [84]. (d) Примеры производных Pt(IV) тройного действия цисплатина, содержащих DCA (красный), производные цисплатина (черный) и ингибиторы COX (зеленый) [85]. (e) Химическая структура DPB, содержащего DCA (красный), биотин (синий) и комплекс платины (Pt) (черный) [86].
Другие предлагаемые механизмы действия DCA
Метаболический сдвиг от гликолиза к окислению глюкозы из-за ингибирования PDK и последующей активации PDH является наиболее известным и общепринятым молекулярным эффектом введения DCA. Последующие биохимические изменения, включая увеличение ROS и изменение потенциала митохондриальной мембраны, могут быть ответственны за остановку пролиферации и гибель раковых клеток, тем самым объясняя полезный потенциал DCA в лечении рака [9] . Однако молекулярные промежуточные продукты, активируемые после введения DCA, до сих пор неизвестны. Вполне возможно, что такая малая молекула может напрямую или косвенно влиять на другие клеточные и молекулярные мишени (рисунок 3), демонстрируя другие механизмы действия, чтобы объяснить ее эффективность также в клеточных моделях, где она не производит ожидаемого метаболического сдвига [12] . Протеомный подход, примененный к клеткам рака легких, продемонстрировал способность DCA увеличивать концентрацию каждого промежуточного продукта TCA, при этом он не влиял на поглощение глюкозы или гликолитический процесс от глюкозы до пирувата [87] . В попытке пролить свет на механизм действия DCA, Дюбуа и коллеги использовали подход, основанный на метаболомике, на нескольких линиях клеток рака яичников, обработанных DCA, и обнаружили общее заметное истощение внутриклеточного пантотената, предшественника CoA, а также сопутствующее увеличение CoA, что предполагает способность DCA увеличивать биосинтез CoA de novo. Поскольку высокие концентрации CoA оказались токсичными для клеток, этот метаболический эффект может быть ответственен за токсичность раковых клеток, опосредованную DCA [88] . Совсем недавно работа Эль Сайеда и соавторов представила новую основанную на доказательствах гипотезу, предполагающую, что эффективность DCA против рака может быть обусловлена его способностью противодействовать ацетату [89] , который, как известно, является энергетическим субстратом для глиобластомы и метастазов в мозг, способным усиливать синтез ДНК, РНК и белка, а также посттрансляционные модификации, тем самым способствуя пролиферации клеток и прогрессированию рака. Более того, высокие уровни ацетата связаны с устойчивостью к противораковым препаратам [90] . Было показано, что DCA способен обращать вспять метаболические изменения, вызванные ацетатом, восстанавливая физиологические уровни сывороточного лактата и свободных жирных кислот, а также концентрацию калия и фосфора. По мнению авторов, благодаря структурному сходству с ацетатом, DCA может ингибировать метаболические эффекты, вызванные ацетатом, ответственные за рост раковых клеток и химиорезистентность [89] . Другим возможным дополнительным эффектом DCA может быть модуляция pH. Известно, что модуляция уровня pH влияет на процессы пролиферации и апоптоза [91] , а также на чувствительность к химиотерапии [92].Обработка DCA может как увеличивать, так и уменьшать внутриклеточный pH. Вторичным эффектом перенаправления пирувата в митохондрии с помощью DCA будет снижение лактата и последующее увеличение внутриклеточного pH. С другой стороны, DCA способен уменьшать экспрессию монокарбоксилатных транспортеров и V-АТФазы с последующим снижением pH, и это особенно происходит в опухолевых клетках, экспрессирующих большее количество этих переносчиков по сравнению с нормальными аналогами [93] . Учитывая способность вызывать быстрое внутриклеточное закисление опухоли, Albatany et al. [94] предположили о возможном использовании DCA в качестве трекера при визуализации in vivo мышиной модели глиобластомы и поддержали терапевтическое использование DCA, поскольку известно, что внутриклеточное закисление вызывает активацию каспазы и фрагментацию ДНК раковых клеток [95] . Животные модели позволяют идентифицировать возможную дополнительную молекулярную мишень DCA. Эксперименты, проведенные на крысах, подчеркнули способность DCA ингибировать экспрессию почечного котранспортера Na-K-2Cl (NKCC) в почках крыс [96] . Поскольку NKCC является важным биомаркером регуляции внеклеточного и внутриклеточного ионного гомеостаза и участвует в прогрессировании клеточного цикла, он играет важную роль в пролиферации раковых клеток, апоптозе и инвазии. Белкахла и др. [97] исследовали взаимодействие между таргетингом метаболизма и экспрессией транспортеров ABC, ответственных за экспорт лекарств из клеток и последующую множественную лекарственную устойчивость, и обнаружили, что лечение DCA способно снизить экспрессию генов и белков транспортеров ABC в нескольких опухолевых клетках, экспрессирующих дикий тип p53, как in vitro, так и in vivo [98] . Уже была продемонстрирована способность DCA вызывать дифференциацию посредством модуляции взаимодействия PKM2/Oct4 в клетках глиомы [99] . Полученное снижение уровней транскрипции Oct4 было связано с уменьшением фенотипа стволовости и значительным повышением чувствительности к клеточному стрессу. Это наблюдение позволяет предположить потенциальную роль DCA против раковых стволовых клеток (CSC).
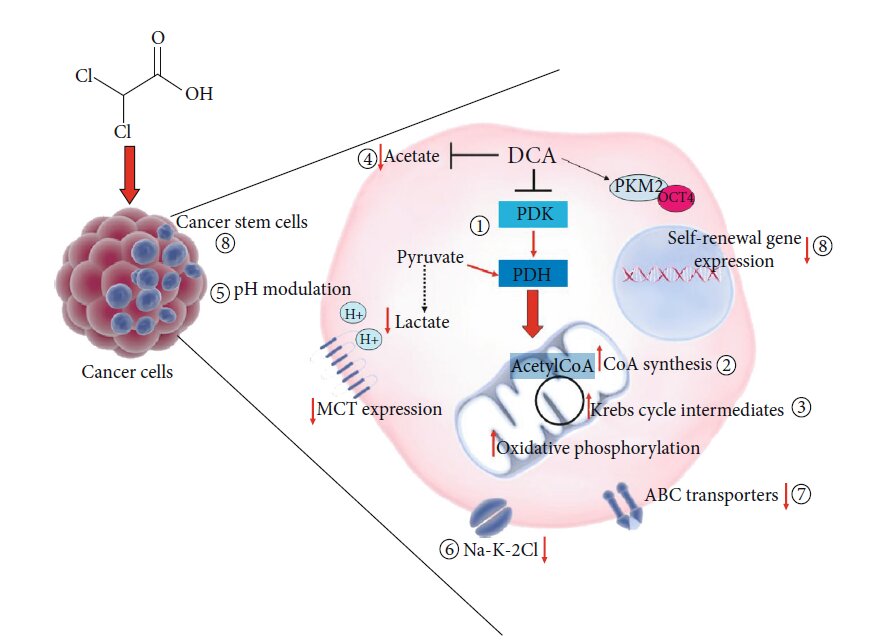 Рисунок 3: Другие предлагаемые механизмы действия DCA. Основной механизм действия DCA заключается в ингибировании пируватдегидрогеназной киназы (PDK), что приводит к активации пируватдегидрогеназы (PDH) и содействует окислительному фосфорилированию (1). DCA также увеличивает концентрацию промежуточных продуктов каждого цикла Кребса (2) [87]. DCA вызывает токсичность клеток посредством синтеза CoA de novo (3) [88]. DCA может противодействовать ацетату (4) [90]. DCA модулирует внутриклеточное закисление (5) [93, 94]. DCA ингибирует котранспортер Na-K-2Cl (6) [96]. DCA подавляет экспрессию генов и белков транспортеров ABC (7) [97]. DCA снижает экспрессию генов, связанных с самообновлением, и влияет на фракцию стволовых клеток рака (8) [99].
Рисунок 3: Другие предлагаемые механизмы действия DCA. Основной механизм действия DCA заключается в ингибировании пируватдегидрогеназной киназы (PDK), что приводит к активации пируватдегидрогеназы (PDH) и содействует окислительному фосфорилированию (1). DCA также увеличивает концентрацию промежуточных продуктов каждого цикла Кребса (2) [87]. DCA вызывает токсичность клеток посредством синтеза CoA de novo (3) [88]. DCA может противодействовать ацетату (4) [90]. DCA модулирует внутриклеточное закисление (5) [93, 94]. DCA ингибирует котранспортер Na-K-2Cl (6) [96]. DCA подавляет экспрессию генов и белков транспортеров ABC (7) [97]. DCA снижает экспрессию генов, связанных с самообновлением, и влияет на фракцию стволовых клеток рака (8) [99].
DCA и раковые стволовые клетки
Растет интерес к таргетированию раковых стволовых клеток (CSC), которые, по-видимому, являются основной причиной рецидива опухоли [100] . CSC обладают способностью к самообновлению с нормальными стволовыми клетками и могут давать начало дифференцирующимся клеткам, ответственным за возникновение опухоли, а также злокачественную прогрессию [101] . Низкая скорость пролиферации и специфический метаболический профиль способствуют тому, что CSC становятся устойчивыми к традиционной химиотерапии [102] . Возникла острая необходимость в разработке новых терапевтических средств, способных влиять на жизнеспособность раковых стволовых клеток [103] с целью полного уничтожения опухолевой массы. Обширный объем литературы фокусирует внимание на метаболическом фенотипе CSC, которые, по-видимому, отличаются от дифференцированных раковых клеток и могут представлять собой терапевтическую мишень [104–108] . В этой ситуации была выдвинута гипотеза о возможной чувствительности фракции CSC к DCA, которая была протестирована на различных моделях рака. Эмбриональные стволовые клетки карциномы представляют собой одну из наиболее подходящих моделей для изучения поддержания и дифференциации CSC, а также идентификации препаратов и молекул, способных модулировать эти процессы [109] . Исследования, проведенные на эмбриональных стволовых клетках (ESC), представляют собой предварительные важные доказательства, подтверждающие возможную эффективность DCA [110] . Интересно, что обработка ESC DCA способствует потере плюрипотентности и сдвигает их в сторону более активного окислительного метаболизма, что сопровождается значительным снижением экспрессии HIF1a и p53 [111] . Вега-Наредо и др. [112] описали важность митохондриального метаболизма в управлении стволовостью и дифференциацией в такой модели. Они охарактеризовали метаболический профиль фракции стволовых клеток и предположили меньшую восприимчивость фенотипа ствола к митохондриально-направленной терапии. Принуждение CSC к окислительному метаболизму путем обработки DCA позволило перейти от стволовости к дифференциации. Несколько отчетов подтверждают существование CSC в глиоме [113, 114] , и эффективность DCA для поражения CSC была широко оценена при таком типе рака, который так трудно лечить обычными методами и который характеризуется низкими показателями выживаемости. Еще в 2010 году Микелакис и коллеги предположили, как in vitro, так и in vivo, способность DCA вызывать апоптоз фракции стволовых клеток рака [26] . Модель глиомы на крысах, повторяющая несколько особенностей человеческой глиобластомы, подтвердила эффективность DCA для потенцирования апоптоза CSC глиомы, характеризующегося значительной сверхстимуляцией гликолитического пути по сравнению с нормальными стволовыми клетками [115]. Кроме того, Цзян и др. исследовали влияние DCA на небольшую популяцию стволовых клеток глиомы (GSC), выделенных из глиобластомы, продемонстрировав снижение свойств самообновления и увеличение процента гибели клеток [44] . Более того, тест in vivo на мышах с ксенотрансплантатами, полученными из GSC, обработанных DCA, показал значительное увеличение общей выживаемости. Лечение DCA также было протестировано на фракции стволовых клеток меланомы, и полученная биоэнергетическая модуляция смогла противодействовать протуморогенному действию ингибитора c-Met [116] . Совсем недавно проведенная работа на гепатоцеллюлярной карциноме человека выявила сверхэкспрессию PDK4 в сферах, происходящих из раковых клеток, с определенным фенотипом, подобным стволовому. Интересно, что лечение DCA смогло снизить жизнеспособность как раковых дифференцированных клеток, так и раковых стволовых клеток и обратить вспять химиорезистентность к традиционной терапии [36] . Наша группа недавно испытала способность DCA снижать экспрессию маркеров стволовых клеток рака CD24/CD44/EPCAM в клеточной линии рака поджелудочной железы, а также нарушать образование и жизнеспособность сфероидов [12] , что дополнительно подтверждает данные, полученные в других моделях рака. Наряду с химиорезистентностью, радиорезистентность также представляет собой ограничение эффективного лечения рака, и CSC, по-видимому, ответственны за такую рефрактерность [117] . Сан и др. продемонстрировали способность DCA повышать радиочувствительность клеток медуллобластомы, влияя на стволоподобные клоны, снижая процент экспрессии CD133-позитивных клеток и уменьшая образование сфер [72] . Более того, в той же клеточной модели они показали измененный механизм репарации ДНК, вызванный DCA, способный объяснить повышенную эффективность радиотерапии.
Выводы
Нацеливание на метаболизм раковых клеток представляет собой новый фармакологический подход к лечению рака. Способность DCA переключать метаболизм с гликолиза на окислительное фосфорилирование увеличила интерес к этому препарату, уже известному своими противораковыми свойствами. Накопленные за последние годы доказательства подтверждают способность DCA преодолевать химио- и радиорезистентность при нескольких типах рака и позволяют выдвинуть гипотезу о дополнительных клеточных мишенях, способных объяснить его способность убивать раковые клетки. Необходимо разработать дальнейшие клинические исследования, которые в настоящее время ограничены пациентами с плохим прогнозом и запущенными рецидивирующими новообразованиями, уже не поддающимися другим традиционным методам лечения. Его потенциальная эффективность против раковых стволовых клеток, а также разработка новых лекарственных форм приближают нас к достижению эффективного клинического применения DCA.
Конфликты интересов
Авторы заявляют об отсутствии конфликта интересов.
Благодарности
Данная работа была поддержана Текущими исследовательскими фондами Министерства здравоохранения Италии в IRCCS-CROB, Рионеро-ин-Вультуре, Потенца, Италия.